Yderst succesfuldt symposium om periimplantitis
”Periimplantitis – fra en kirurgisk, protetisk og parodontologisk vinkel” var titlen på årets symposium, og det leverede arrangementet til fulde, for de fagligt ansvarlige Christian Damgaard, Simon Storgård Jensen og John Orloff havde sammensat et alsidigt og attraktivt program, hvor nogle af verdens førende forskere og klinikere fra Europa og Australien formidlede deres emner og budskaber inden for feltet. Det blev til to fantastiske og udbytterige dage for de 660 deltagere den 4.-5. november i Scandic Falkoner Frederiksberg.

Da flere og flere af de patienter, som vi møder i praksis, har fået erstattet manglende tænder med implantater, og ca. 20 % af disse patienter udvikler periimplantitis, er sandsynligheden for, at en patient, som kommer i din tandklinik, med mindst et tandimplantat høj og måske med periimplantitis. Derfor var det et længe ventet og yderst relevant emne for hele klinikteamet, dette års symposium præsenterede.
De fagligt ansvarlige havde på forhånd opstillet nogle fokusspørgsmål, som blev besvaret i løbet af dagene:
Har den biologiske opbygning af de periimplantære væv indflydelse på progressionen af periimplantitis?
Der er store forskelle på de periimplantære væv sammenlignet med de parodontale væv omkring tænder. Implantat mangler karakteristiske tandstrukturer såsom rodcement, parodontalligament, dentoalveolære og dentogingivale fibre. Omkring implantatet består bindevævet af parallelorienterede fibre. Det er et mindre vaskulariseret og fibrøst væv analogt til arvæv. Disse anatomiske forskelle er bl.a. medvirkende til, at den periimplantære mucosa er mindre udrustet til at modstå biofilmdannelsen, hvilket er en af årsagerne til, at periimplantitis progredierer hurtigere og mere aggressivt end parodontitis. Særligt fraværet af parodontalligamentfibrene medfører større inflammatorisk læsion omkring den periimplantære mucosa samt manglende begrænsning af læsionen fra den underliggende knogle.
Hvordan diagnosticeres periimplantære sygdomme?
Ved periimplantær sundhed danner det omkringliggende blødtvæv en beskyttende forsegling omkring den transmukosale del af implantatet – abutmentdelen af restaureringen. En streng af bindevæv dækkes af keratiniseret epitel. Efter implantatindsættelse optræder let marginal knoglemodellering.
Ved ”World Workshop 2017” blev periimplantære sygdomme og tilstande klassificeret og inddelt i periimplantær sundhed, mucositis og periimplantitis (Faktaboks 1) (1). Her defineres periimplantær sundhed som fravær af blødning ved sondering samt fravær af knogletab udover marginale knogleniveauforandringer som resultat af den initiale knogleremodellering. Periimplantitis er karakteriseret ved inflammation omkring det periimplantære væv med fordybede pocher (> 6 mm) samtidig med progressivt tab af den støttende knogle (> 2 mm). Et bud på klassifikationen af periimplantære knogledefekter kan ses på Fig. 2.
På trods af de anselige forskelle på de periimplantære væv og parodontale væv er det bedste diagnostiske redskab, vi har på klinikken, fortsat pochemåleren til at diagnosticere periimplantære sygdomme (blødning/pus og pochedybdeforandringer), og den bør benyttes ved hvert besøg på klinikken til sammenligning med udgangsmåling ved suprastrukturens påsættelse.

Er der systemiske og lokale risikofaktorer, der kan være medvirkende årsager til udviklingen af periimplantitis?
Der var bred enighed blandt foredragsholderne om, at den orale biofilm anses for at være den ætiologiske faktor for udviklingen af periimplantitis. Studier viser, at dårlig plakkontrol og fravær af regelmæssig vedligeholdelsesterapi øger risikoen for periimplantitis. Samtidig er en antiinfektiøs behandlingsstrategi af periimplantitis succesfuld til at mindske inflammationen i blødtvæv og undertrykke sygdomsprogressionen.
Systemiske risikofaktorer er faktorer, som ændrer individets modtagelighed overfor sygdom. Det er biologisk sandsynligt, at individer, der er rygere, lider af diabetes mellitus og parodontitis (BOP > 10 %, PPD > 5 mm) samt er behandlet for parodontitis, har øget risiko for udvikling af periimplantitis. Lokale risikofaktorer kan være medvirkende årsag til periimplantitis. De inddeles i blødtvævsfaktorer, hårdtvævsfaktorer og protetiske aspekter (Faktaboks 2).
Forebyggelse er nøglen til at reducere risikoen for periimplantitis. Heitz-Mayfield et al. 2020 (2) har udarbejdet et godt redskab, som kan benyttes til bestemmelse af en patients risikoprofil for udvikling af periimplantitis (Implant Disease Risk Assessment – IDRA). Otte parametre er foreslået, hver af dem er kategoriseret i henholdsvis lav-, medium- eller højrisiko.
Påvirker implantatoverfladen risikoen for periimplantitis?
For ca. 50 år siden lancerede Brånemark og Schroeder deres titaniumimplantater. De havde to forskellige tilgange, som begge var meget succesfulde. Et system med glat overflade og forsinket heling og et andet med en meget ru overflade og transmukosal heling. Siden da har alle eksisterende implantatsystemer introduceret nye overflader og design, og i dag er der mange forskellige implantatoverflader på markedet, som alle er med ru overflader. Modifikationerne af overfladernes topografi, både fysisk og kemisk, har vist sig at have udtalt effekt med stigende osseointegrationshastighed, bedre mekanisk stabilitet og større mængde af mineraliseret BIC (Bone to Implant Contact). Omvendt kræver det, at en glat overflade møder blødtvævet.
Der er ingen forskel på forekomsten af periimplantitis på forskellige implantatoverflader eller materialer. Derimod er der ved ligaturinducerede periimplantitisstudier vist, at progressionen af periimplantitis er mere udtalt ved implantater med ru overflade end implantater med glat overflade. Det indikerer, at modificerede overfladekarakteristika kan have en signifikant negativ indvirkning på progressionen af periimplantitis.
Behandlingsudfaldet ved periimplantitis er forskelligt, alt efter om implantatet har en ru eller glat overflade. Foretages lapkirurgi, kan de ru implantater have gavn af systemisk antibiotikum. Gældende for alle patienter med implantater er, at stringent støttende vedligeholdelsesprotokoller er obligatoriske.

Påvirker implantatdesign risiko for periimplantitis?
Hovedforskellen på implantatdesign er ”bone-level” design eller ”tissue-level” design. Tissue-level design har en glat poleret hals supracrestalt, og den intraossøse del har en ru overflade. Dette implantat løfter den restaurative platform væk fra knoglen, hvilket tillader bedre visualisering, lettere tilgang til kronen og vedligeholdelse. Implantater med kronekanter, som ligger > 1,5 mm fra knoglekanten, udviser mindre periimplantitis sammenlignet med ”bone level” implantater, hvor den restaurative margin ligger tættere på knoglen. Derudover kan tissue-level implantater have en fordel, hvor der forventes højt stressniveau, fx ved restaureringer med ekstentionsled eller høj krone-til-implantatratio grundet deres bedre kraftfordeling.

Det tyder på, at geometrien af skruegangen har indflydelse på effekten af dekontaminerings-effektiviteten; implantater med lave skruegange er lettere at dekontaminere. Nogle gange er det nødvendigt at fjerne implantatet, og her kan implantatdesignet have indflydelse. Fx er korte implantater lettere at fjerne end lange.
Anbefalinger:
• Modificerede/ru overflader for knogleintegration.
• Flyt mikrospalter væk fra knoglen, og den glatte overflade i den periimplantære sulcus vil reducere risikoen for periimplantitis.
• Primær forebyggelse for at opretholde blødtvævsforseglingen og undgå eksponering af implantatets ru overflade, da det kan have indflydelse på progressionen af periimplantitis.
• Overvej tissue-level implantater til modtagelige patienter, fx parodontitispatienter (Fig. 3).
Kan suprastrukturens udformning eller materialevalg forebygge eller inducere periimplantitis?
Der er ingen klinisk signifikant forskel på knogle-og blødtvævsniveau trods gentagne abutmentindprøvninger eller mikrobevægelser, men at undgå dem kan være en fordel. Platform switching design kan muligvis hindre marginal remodellering. Mht. abutmentmateriale er der ingen signifikant forskel på, om der benyttes metal eller keramiske abutments på den periimplantære sundhed. Heller ikke på valget af materiale og overfladebehandlingen af den protetiske rekonstruktion synes der at være en forskel. Dog efterlades den marginale del af kronen fortsat som poleret zirconium uden farve og glans.
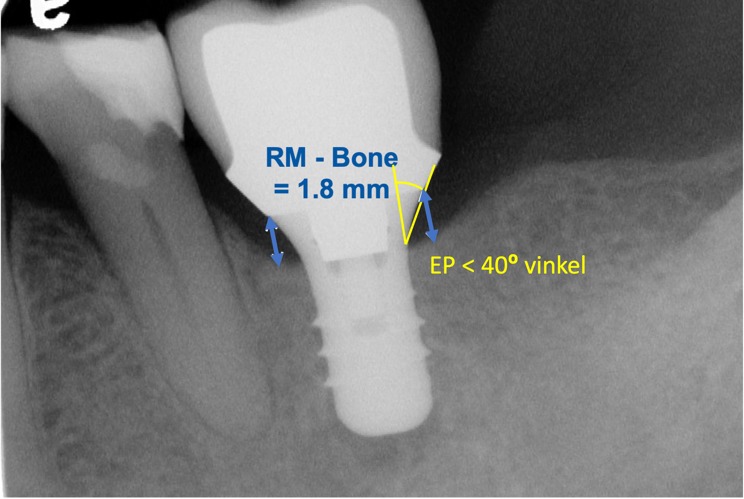
I forhold til abutmentdesignet er det som tidligere beskrevet vist, at den restaurative vinkel kan have afgørende betydning på tilstedeværelse eller fravær af marginalt knogletab. Bred og flad restaurativ vinkel (> 40o) inducerer apikal forskydning af den periimplantære biologiske bredde og mere knogletab sammenlignet med smalle abutments. Flaskehalsdesign er at foretrække. Det er en god idé at indtegne på røntgenbilledet til din tekniker, således at korrekt smalle design opnås (Fig. 3). Mikrobevægelser mellem ikke originale abutments og implantatet kan medføre marginalt knogletab – anvend originale abutments.
Er opbygning af hårdt- og blødtvæv en forudsætning eller en risikofaktor for periimplantitis?
Ved manglende bukkal knogle og vertikalt knogletab i bukkolingval dimension ses hyppigere knogletab og periimplantitis til følge. Derfor er opbygning af den bukkale knogle nødvendig enten under eller før implantatindsættelse. Jo tykkere den er, jo bedre mukosal æstetik og vaskularisering, men som minimum 1,5 mm.
I forhold til det æstetiske udfald, hvilket ofte er prioriteret i den anteriore zone af tandsættet, ønskes ofte rimelig mukosal tykkelse. For at opnå dette benyttes et bindevævstransplantat. Dette vil øge blødtvævstykkelsen, hvilket dog ikke er associeret med forbedret periimplantær sundhed. Derimod er bredden af den keratiniserede mucosa (< 2 mm) associeret med periimplantær sygdom og patientubehag. Her anbefales apikalt positioneret lap og placering af frit gingivalt transplantat. Tidspunktet for behandlingen kan foregå under eller efter implantatindsættelse. Vær opmærksom på den større skrumpning af det frie gingivale transplantat ved implantater i forhold til tænder. Spontan keratiniseret mucosa dannes ikke omkring implantater grundet manglende parodontalligament. Ydermere inducerer et bindevævstransplantat heller ikke ny keratiniseret mucosa omkring implantater. Dannelsen af keratiniseret mucosa kan positivt ændre prognosen for implantatets sundhed.
Hvordan kan periimplantitis behandles?
Når der forekommer periimplantitis, er skruegangene og de ru/modificerede overflader eksponeret til blødtvæv og udenfor knoglen. Det primære mål for behandlingen af periimplantitis er infektionskontrol og hvis muligt at opretholde implantatet i funktion. Systematisk tilgang til behandlingen er nødvendigt.
Trin 1
Patienten forberedes inden kirurgi med mundhygiejneinstruktion, polering med gummikop evt. airflow.
Trin 2
Kirurgisk behandling af periimplantitis med adgangsgivende lapoperation, fjernelse af granulationsvæv (overfladedekontaminering ved anvendelse af titaniumcuretter) og NiTi pensel/titaniumbørster. Ingen airflow, da det ikke er godkendt under kirurgi.
Systemisk antibiotikum har en signifikant positiv effekt på behandlingen særligt ved implantater med ru/modificerede overflader.
Rekonstruktive teknikker (knoglegraft/membran) versus adgangsgivende lapoperation viser, at der ingen signifikant forskel er på pochedybde og BOP. Kirurgisk behandling af periimplantitis kan effektivt forbedre den kliniske og radiologiske status (1-3 års data). Patienttilfredsheden er høj. Brug af knoglesubstitutter forbedrer ikke sygdomshelbredelsen, dog ses mindre bukkal blødtvævsretraktion, hvilket kan forbedre det æstetiske udfald.
Der er delte holdninger til, om skruegangene skal fjernes ved implantoplastik, da litteraturen fortsat er sparsom. Rationalet bag fjernelse af skruegangene er at efterlade en mere glat implantatoverflade eksponeret til mundhulen efter knogledestruktion som følge af periimplantitis. Her anbefales tungsten karbidbor efterfulgt af silikonepolering. Der sås tvivl om, hvorvidt de titaniumpartikler, som efterlades i vævet, gør skade, samt om der sker svækkelse af implantaterne. Behandlingen med implantoplastik bør overvejes primært ved horisontale og brede knogledefekter (Fig. 2, klasse II/III) for efterfølgende at lette adgangen til optimal kontrol af mundhygiejne.
I nogle tilfælde er eksplantation af implantatet den bedste behandling af periimplantitis og bør overvejes ved knogletab > 50 %, ekstrem malposition af implantatet eller implantatfraktur.

Fremtiden med periimplantitis – bliver vi gladere med alderen særligt efter de 50?
I takt med at levealderen stiger, og der bliver flere og flere ældre med egne tænder og implantater, vil vi i fremtiden skulle håndtere behandlingen af periimplantitis. En implantatunderstøttet protese (hybridprotese) har en række fordele for den ældre. Bl.a. er den med til at hindre atrofi af knogle, tab af muskelstyrke, opretholde taktil sensitivitet, muskelkoordination og tyggekraft og dermed bedre ernæringsstatus. Ydermere giver den øget selvværd og velbefindende. Selvom der er en masse følgesygdomme, som følger med alderen (hjerte-kar-sygdomme, nedsat immunforsvar, svækket nervesystem, syn, taktilitet samt muskelkraft), som kan kompromittere brugen af implantater samt også give spekulationer om periimplantitis, er det den nye geriatriske gigant? Så ser det ikke ud til at være et problem endnu. Implantatsucceskriterier er patientens evne til håndtering af den protetiske rekonstruktion, og derfor i takt med stigende alder at anvende ”back off”-strategien med at gå fra faste rekonstruktioner til aftagelige rekonstruktioner, herunder hybridproteser hos nogle patienter ved eventuelt ovenikøbet at sætte implantaterne på standby (fjerne attachment og placere helingskapper). Igen, den vigtigste parameter for sunde periimplantære forhold er patientens evne til renhold.
Og med dette års symposium har vi taget det første skridt i den retning. Faktaboks 3 viser højdepunkter fra symposiet, og husk på: at ”Jo mere vi ved, des mindre ved vi, at vi ved.”

Litteratur
1. Berglundh T, Armitage G, Araujo MG et al. Peri-implant diseases and conditions: Consensus report of workgroup 4 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol 2018;89 (Supp1);S313-8.
2. Heitz-Mayfield LJA, Heitz F, Lang NP. Implant disease risk assessment IDRA – a tool for preventing peri-implant disease. Clin Oral Implants Res 2020;31:397-403.